من خصائص الفلزات
من خصائص الفلزات، هناك العديد من الخصائص للمعادن التي تميز هذه المواد عن غيرها من اللافلزات وشبه المعادن، حيث يوجد العديد من المواد والعناصر التي قسمها العلماء إلى مجموعات بمرور الوقت، تختلف كل منها عن الأخرى على الأرض، وهي معادن وغير المعادن سوف نشرح خصائصها لك.
من خصائص الفلزات
المعادن هي مواد تتميز بارتفاع درجة حرارتها وتوصيلها الكهربائي الجيد، بالإضافة إلى قابليتها للتشكيل والليونة في درجات حرارة عالية وقدرتها العالية على عكس أشعة الضوء، وهي ثلاثة أرباع إجمالي العناصر الكيميائية على الكوكب ومن أكثرها شيوعًا و المعادن الأكثر انتشارًا في قشرة الأرض هي المغنيسيوم والبوتاسيوم والصوديوم والكالسيوم والحديد والألمنيوم، وسنقوم بتفكيك خصائص المعادن في ما يلي
الخصائص الفيزيائية للفلزات
تشمل أشهر وأهم الخواص الفيزيائية للمعادن ما يلي
- الرنين توصف المعادن بأنها رنين عالي أو ضوضاء عند اصطدامها بأشياء أو مواد صلبة.
- واللمعان تتميز جميع المعادن بمظهرها اللامع اللامع، وبعضها موجود أيضًا في الطبيعة بدون هذه الخاصية بسبب الظروف الطبيعية والبيئية التي تتعرض لها ويمكن صقلها لمنحها اللمعان مرة أخرى ومظهرها اللامع.
- ثم المرونة وتعني قدرة المواد المعدنية على التكون والتمدد بالشكل الذي تتعرض فيه لدرجة الحرارة العالية، بالإضافة إلى متانة ما بعد التشكيل، مما يجعل الكابلات من المعادن بتعريضها لدرجة حرارة عالية ثم سحبها. بجانب استخدام المعادن لاغراض اللحام.
- القابلية للتشكيل هي خاصية المعادن التي يمكن ضربها وتشكيلها إلى صفائح مسطحة، والأمثلة في هذا السياق هي صفائح الألمنيوم، وتستخدم المعادن في صناعة الطائرات لقوتها وخفة وزنها، وتستخدم في صناعة الطائرات. صناعة الأواني والسيارات المستعملة ، و اكثر بكثير.
- والموصلية العالية جميع المعادن موصلة جيدة للكهرباء والحرارة، وهذا هو سبب استخدامها في صناعة أواني الطهي بسبب الموصلية الحرارية العالية.
الخواص الكيميائية للفلزات
نقدم في النقاط التالية أهم الخواص الكيميائية للمعادن
- التفاعل مع الأكسجين عند احتراق المعادن في وجود عنصر الأكسجين، تتشكل أكاسيد المعادن، وتحدث المعادن بشكل طبيعي في شكل أكاسيد، على سبيل المثال في إنتاج أكسيد المغنيسيوم من احتراق عنصر المغنيسيوم مع توافر عنصر الأكسجين.
- والتفاعل مع القواعد لا تتفاعل كل أنواع المعادن مع القواعد، وما يتفاعل معها ينتج غاز الهيدروجين والأملاح المعدنية، كما يحدث عندما يتفاعل هيدروكسيد الصوديوم القوي مع الزنك لإنتاج غاز الهيدروجين وصوديوم الزنك.
- ثم التفاعل مع الأحماض ينتج غاز الهيدروجين عن طريق تفاعل المواد الحمضية مع المعادن، مثل تفاعل حمض الهيدروكلوريك مع الزنك لتكوين غاز الهيدروجين وكلوريد الزنك.
- التفاعل مع الماء يمكن للمعادن النشطة فقط أن تتفاعل مع الماء، بينما المعادن الخاملة غير قادرة على هذا التفاعل، ومن الأمثلة على ذلك تفاعل الصوديوم مع الأكسجين والماء النشط، وتؤدي هذه العملية إلى توليد طاقة حرارية عالية هذا يخزن الكيروسين في حاويات لمنع الرطوبة أو الاتصال بالأكسجين والتفاعل معه.
ما هي خصائص اللافلزات
اللافلزات هي تلك المواد التي تتميز بعدم قدرتها على توصيل المواد الكهربائية أو غير النشطة من حيث طاقة التفاعل، بحيث تنتمي إلى المواد العازلة ذات الموصلية المنخفضة، بما في ذلك أشباه الموصلات ذات الموصلية المعتدلة، ومع ارتفاع درجة الحرارة تزداد موصليةها، وما شابه ذلك المعادن فيما يتعلق بحدوثها في الطبيعة، فيما يلي شرح للحالات الثلاث للمادة الصلبة والسائلة والغازية، والخصائص الفيزيائية والكيميائية لغير المعادن
الخصائص الفيزيائية للا فلزات
هناك العديد من الخصائص الفيزيائية لللا فلزات وأشهرها
- الموصلية المنخفضة من المعروف أن المواد غير المعدنية لها موصلية منخفضة للكهرباء والحرارة، باستثناء الجرافيت.
- وقلة اللمعان واللمعان اللافلزات هي عناصر معتمة وليست لامعة ولا لامعة.
- ثم غير طنين عندما تصطدم غير المعادن بأجسام صلبة، فإنها لا تصدر صوتًا طنينًا.
- لا تتسامح مع الانحناء أو التشكيل تتميز المواد غير المعدنية بعدم القدرة على الانحناء أو تكوينها، ومن المستحيل الضرب أو السحب على شكل صفائح معدنية بسبب تكسيرها وهشاشتها العالية تحت الضغط.
- وعدم المرونة تتميز اللافلزات بأنها مادة ناعمة لا يمكن سحبها وتشكيلها على شكل أسلاك، باستثناء مادة الكربون وهي من المواد التي تأخذ شكلاً وتتميز بالليونة مما يجعل يمكن إنتاج ألياف الكربون التي يسهل الخروج منها.
الخواص الكيميائية للا فلزات
ومن أبرز الخصائص الكيميائية للمعادن نذكر ما يلي
- التفاعل مع الأكسجين تتشكل أكاسيد اللافلزات عندما تتفاعل مع عنصر الأكسجين، وهو مادة محايدة أو حمضية.
- والتفاعل مع القواعد التفاعل الذي يحدث في التفاعلات المعقدة بين المواد الأساسية وغير المعدنية، على سبيل المثال تفاعل هيدروكسيد الصوديوم مع الكلور لتكوين كلوريد الصوديوم وهيبوكلوريت الصوديوم والماء.
- ثم التفاعل مع الأحماض جميع غير المعادن لديها القدرة على التفاعل مع المواد الحمضية.
- التفاعل مع الماء لا يمكن للمعادن أن تتفاعل مع الماء وعادة ما تتفاعل مع الهواء، وتخزن بعضها في الماء.
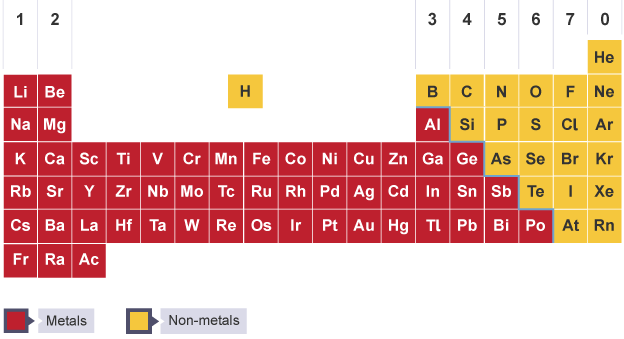
عناصر الفلزات واللافلزات في الجدول الدوري
في الأقسام التالية سوف نعرض لكم مواقع المعادن واللافلزات في الجدول الدوري
موقع الفلزات في الجدول الدوري
توجد المعادن على يسار ووسط الجدول الدوري وتنقسم إلى مجموعات على النحو التالي
- الفلزات القلوية تشمل هذه المجموعة الهيدروجين في الحالة المعدنية والفرانسيوم والسيزيوم والروبيديوم والبوتاسيوم والصوديوم والليثيوم.
- ومعادن الأرض القلوية تشمل هذه المجموعة الراديوم والباريوم والسترونتيوم والكالسيوم والمغنيسيوم والبريليوم.
- ثم المعادن الأساسية تنتمي Tencennes، Lebermorium، Moscovium، Flarovium، Nihonium، البزموت، الرصاص، الثاليوم، الإنديوم، الغاليوم والألمنيوم إلى هذه المجموعة.
- المعادن الانتقالية تشمل هذه المجموعة لورانس، نوبليوم، مندليفيوم، فيرميوم، بلاتينوم، نبتونيوم، يورانيوم، ثوريوم، لوتيتيوم، إيتيربيوم، ثوليوم، إربيوم، يوروبيوم، سير، نحاس، هاسيوم، دوبيوم، رذرفورديوم، ذهب، بكتين وأكتينيوم، أوزميوم، الرينيوم، التنجستن، التنتالوم، الهافنيوم، اللانثانم، الكادميوم، الفضة، البلاديوم، الروديوم، الروثينيوم، التكنيشيوم، الموليبدينوم، النيوبيوم، الزركونيوم، الإيتريوم، الزنك، النحاس، النيكل، الحديد، الكوبالت، الكوبالت والسكنديوم، النيكل.
موقع اللافلزات في الجدول الدوري
المعادن الموجودة على يمينها في الجدول الدوري، باستثناء الهيدروجين، وهو وحده في أعلى اليسار، وهي مصنفة على النحو التالي
- اللافلزات الأساسية تشتمل هذه المجموعة على عنصر الهيدروجين، والذي يكون أحيانًا معدنًا قويًا، والسيلينيوم، والكبريت، والفوسفور، والأكسجين، والنيتروجين، والكربون.
- والهالوجينات تشمل هذه المجموعة التنيسين والأستاتين واليود والبروم والكلور والفلور.
- ثم الغازات النبيلة وتشمل الأوغانيسون والرادون والزينون والكريبتون والأرجون والنيون والهيليوم.