خريطة مفاهيم الروابط الكيميائية
خريطة مفاهيم الروابط الكيميائية، تسعى الذرات إلى ملء مداراتها الإلكترونية الخارجية في محاولة لترتيب نفسها في أنماط مستقرة في بعض الأحيان يجب عليك الانضمام إلى ذرات أخرى لملء هذه المدارات، هذه الروابط الروابط الإلكترونية، وسنتحدث في هذه المقالة عن الروابط الكيميائية وأنواعها، بالإضافة إلى خريطة المفاهيم.
ما هي الروابط الكيميائية
الروابط الكيميائية هي القوة التي تربط الذرات ببعضها البعض في مجموعات تعرف بالروابط الكيميائية يمكن تصنيف الروابط الكيميائية على أنها إحدى اللبنات الأساسية للكيمياء التي تشرح مفاهيم أخرى مثل الجزيئات والتفاعلات، والتي بدونها سيشعر العلماء بأنهم غير قادرين على تفسير سبب انجذاب الذرات لبعضها البعض أو كيفية تكوين المنتجات بعد حدوث تفاعل كيميائي.
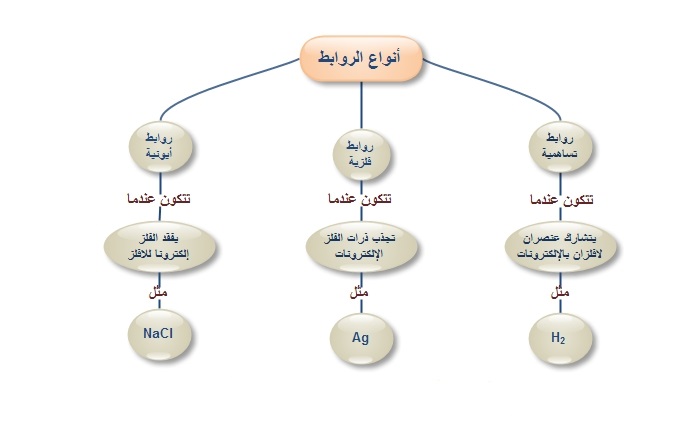
خريطة مفاهيم الروابط الكيميائية
من المعروف أن الذرات المفردة لها حاجة دائمة للاستقرار، لذلك فهي تبحث دائمًا عن روابط كيميائية مع ذرات أخرى للحصول على هذا الثبات والاستقرار، وتختلف طريقة الحصول على ثباتها وفقًا للذرة التي سترتبط بها ، هذه الروابط إما تساهمية (حيث تساهم كل ذرة وتشارك في عدد من الإلكترونات حسب احتياجات كل ذرة) أو روابط أيونية من خلال الخسارة أو الكسب فيما يلي، سنصف خريطة مفاهيمية للروابط الكيميائية.
أنواع الروابط الكيميائية
هناك العديد من الروابط الكيميائية التي تختلف باختلاف حاجة الذرات للإلكترونات، وهذه الأنواع هي
- الروابط الأيونية تشير الرابطة الأيونية إلى الرابطة التي تتضمن نقل الإلكترونات من ذرة إلى أخرى بحيث تكتسب ذرة إلكترونًا بينما تفقد الذرة الأخرى إلكترونًا بحيث يحمل أحد الأيونات الناتجة شحنة سالبة والأيون الآخر يحمل شحنة موجبة، وفقًا للقاعدة، تجتذب الشحنات المعاكسة.
- والروابط التساهمية هي الروابط الأكثر شيوعًا بين الذرات، وهي الروابط التي تساهم مع بعضها البعض في تكوين وتشكيل الجزيء وتنقسم الروابط التساهمية إلى نوعين الرابطة التساهمية القطبية والرابطة التساهمية غير القطبية، أو ما برابطة الهيدروجين.
- ثم الرابطة التنسيق هي حالة وسيطة بين الرابطة الأيونية والرابطة التساهمية، حيث يكون أحد طرفي الجزيء مشحونًا سالبًا والطرف الآخر مشحونًا بشكل إيجابي أيضًا الرابطة التساهمية أو التساهمية تحدث هذه الرابطة بين الذرات لتكوين جزيئات، أو بين ذرة في جزيء وأيون، أو ذرة في جزيء وذرة في جزيء آخر.
- رابطة الهيدروجين تعتبر هذه الرابطة أضعف أنواع الروابط الكيميائية وهي تفاعل يتضمن ذرة هيدروجين تقع بين زوج من الذرات الأخرى التي لها تقارب إلكترون عالٍ في بعض الأحيان توجد هذه الرابطة بين الذرات في جزيئات مختلفة أو في أجزاء من نفس الجزيء.
- والروابط المعدنية القوة التي تربط الذرات في مادة معدنية تتكون هذه المادة الصلبة من ذرات معبأة بإحكام في الروابط المعدنية، يتداخل الغلاف الإلكتروني الخارجي لكل ذرة معدنية مع عدد كبير من الذرات المجاورة، مما يتسبب في انتقال إلكترونات التكافؤ باستمرار من ذرة إلى أخرى، ولا يرتبط بأي زوج محدد من الذرات يمكن وصفه بأنه، على عكس الروابط الموجودة في المواد الرابطة تساهميًا، فهي ليست ثابتة ولديها القدرة على التحرك بحرية نسبيًا في جميع أنحاء البلورة.