في نموذج بور لذرة الهيدروجين يكون إلكترونها في حالة إثارة عندما
في نموذج بور لذرة الهيدروجين يكون إلكترونها في حالة إثارة عندما، تحتوي ذرة الهيدروجين على عدد كبير من الالكترونات، متى يكون الكترون ذرة الهيدروجين في نموذج لها في حالة اثارة، تكون الفيزياء من أهم العلوم التي نستفيد منها وندرسها بطريقة شيقة ومثيرة، الطبيعة الأساسية مثل السرعة والطاقة، سوف نقدمها بإجابة مناسبة على السؤال المطروح.
ما هو نموذج بوهر
في الفيزياء الذرية، يوجد نموذج بوهر، حيث يطلق عليه (الإنجليزية نموذج بوهر)، وهي نواة صغيرة موجبة الشحنة محاطة بالإلكترونات في المدارات باستخدام النظام الشمسي، وذلك لسهولة النموذج، وما زالت موجودة، تستخدم كمقدمة لطلاب الميكانيكا ويسمى، يُطلق على هذا النموذج اسم “نموذج بوهر” نسبة إلى الفيزيائي نيلز بور، الذي تم اقتراحه لتمثيل ذرة الهيدروجين، بحيث يناسب هذا النموذج ويفسر الخطوط الطيفية المنبعثة من ذرات الهيدروجين، يمكن العثور على الإلكترونات في نموذج بوهر على مسافة معينة من البروتونات المرتبطة به، وعندما يكون في مكان آخر، فإنه يتطلب فقد طاقة (إشعاع ضوئي)، فيقل نصف قطر الدوران حول البروتون حتى يسقط فيه، وهذا يؤدي إلى تدمير الذرة، ضوء قوي عند طاقات وترددات معينة.
في نموذج بور لذرة الهيدروجين يكون إلكترونها في حالة إثارة عندما
في الفيزياء سوف تجد نموذج الرافعة الذي يعد من أبرز وأهم النماذج في الفيزياء، لأنه يضم مجموعة من التجارب والدراسات المتنوعة والمختلفة، بالإضافة إلى دراسة الذرة في دراسة كبيرة، لأنها يعتبر أصغر جزء من العنصر، ويتكون بشكل أساسي من النواة، وله دور فعال للغاية في الذرة، حيث تتكون النواة من بروتونات موجبة الشحنة ونيوترونات متعادلة وإلكترونات سالبة، وهناك الكثير من المعلومات التي توضح و يهتم بدراسة الفيزياء لأننا سنجيب على السؤال التالي
- في نموذج بوهر لذرة الهيدروجين، يكون إلكترونها في حالة من الإثارة متى عندما تكتسب جميع الإلكترونات طاقة عالية جدًا.
أهم الأسس التي اقترحها بوهر عام 1913
اقترح بوهر مجموعة من القوانين والأسس والتشريعات التي كتبها لإثبات تجاربه العلمية التي تفيد الكثير من المفكرين في عصرنا لأنهم يبحثون عنها كثيرًا، وكان ذلك في عام 1913، وهذه الأسس على النحو التالي
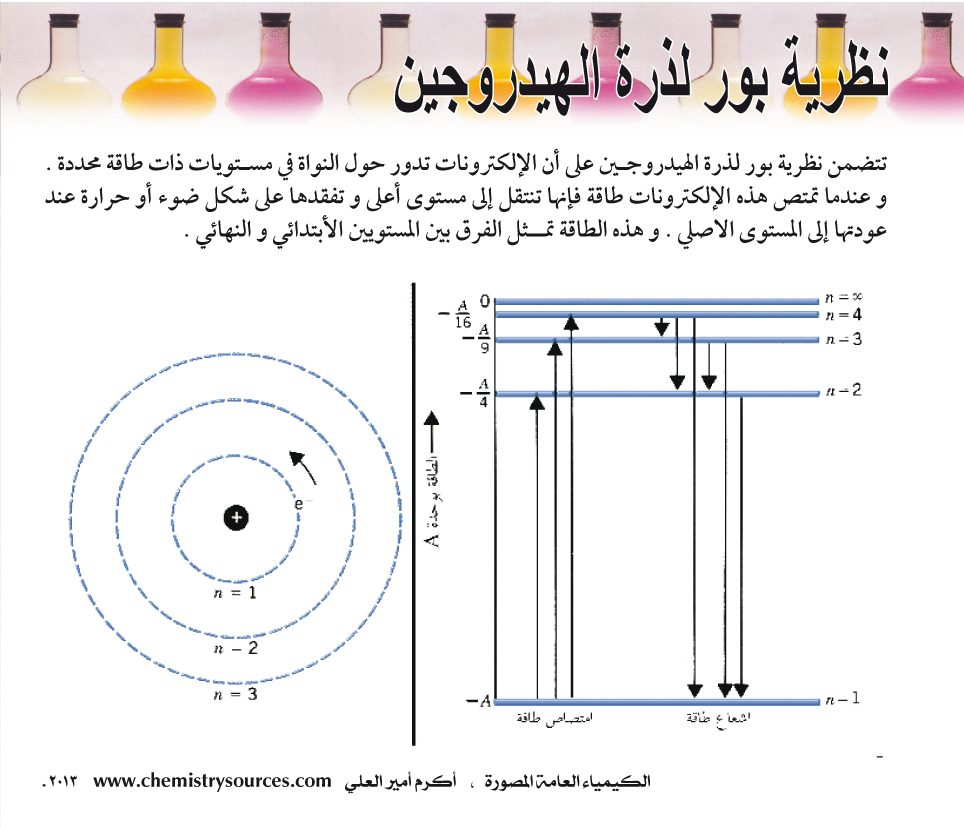
- تدور الإلكترونات حول مدارات دائرية، كل مدار يحتوي على كمية منفصلة من الطاقة التي تدور حول البروتون تحت تأثير قوة جاذبية كولوم.
- لا تنطبق قوانين الميكانيكا التقليدية عندما تقفز الإلكترونات بين المدارات المسموح لها بالوجود فيها، لأنها تنطبق فقط على مدارات الإلكترون الثابتة ولا تصدر طاقة.
- عندما يقفز الإلكترون من مدار إلى آخر، فإن فرق الطاقة إما يفقد أو يكتسب وحدة من الطاقة (تسمى الفوتون)، والتي لها طاقة مكافئة لفرق الطاقة بين المدارين.
- تعتمد المدارات المسموح بها على قيم كلمات الزخم الزاوي الخاصة والمدارية المنفصلة.